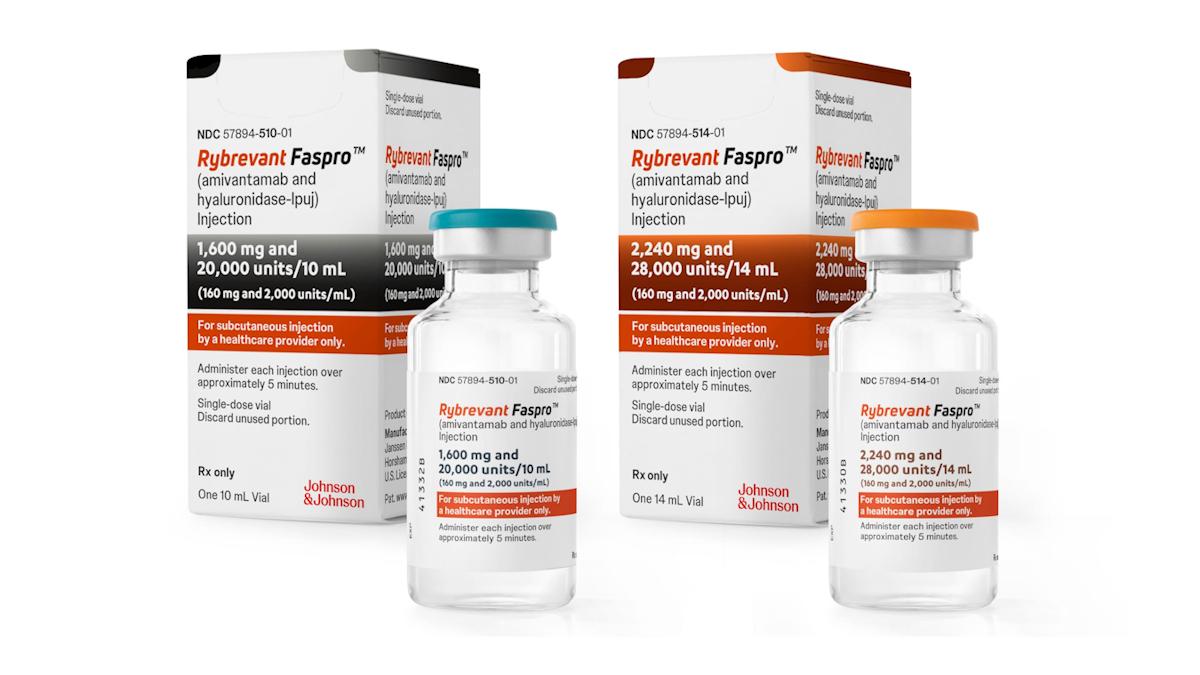
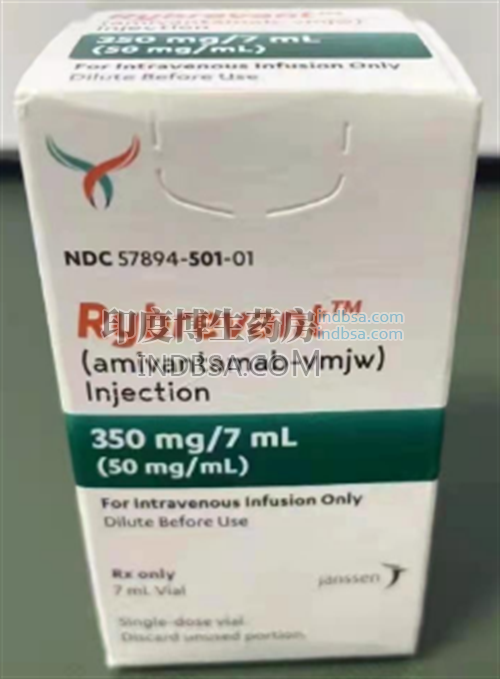
使用Rybrevant时,患者和医疗提供者需要注意以下事项:
1. **输注相关反应(IRR)**:在首次出现IRR体征时中断输注。根据反应的严重程度降低输注速率或永久停用Rybrevant。

2. **间质性
肺病(ILD)/肺炎**:监测指示ILD的新发或恶化症状。疑似ILD/肺炎患者立即停用Rybrevant,如果确诊ILD/肺炎,则永久停药。
3. **皮肤不良反应**:Rybrevant可能引起皮疹,包括痤疮样皮炎和中毒性表皮坏死松解症(TEN)。根据严重程度暂停使用、减少剂量或永久停用Rybrevant。治疗期间和治疗后2个月内限制日光照射,穿防护服,并使用广谱UVA/UVB防晒霜。
4. **眼毒性**:Rybrevant可能引起眼睛问题,如角膜炎、干眼症状、结膜发红、视力模糊、视力损害、眼痒和葡萄膜炎。出现眼部症状的患者应及时转诊至眼科医生,并根据严重程度暂停使用、减少剂量或永久停用Rybrevant。
5. **胚胎-胎儿毒性**:Rybrevant可能导致胎儿损害。建议有生育能力的女性在治疗期间和末次给药后3个月内采取有效的避孕措施。
6. **剂量和给药**:Rybrevant的剂量基于基线体重,不需要根据后续体重变化进行调整。初始剂量应在第1周分两天给药,并且应在每次输注前给予预防药物以降低IRR风险。
7. **禁忌症**:目前没有特别的禁忌症记录。
8. **警告和注意事项**:除了上述提到的,还包括对驾驶和操作机械能力的影响、药物相互作用等。
9. **患者咨询**:确保患者了解与Rybrevant相关的潜在风险和副作用,并遵循医疗提供者的所有指导。
10. **储存条件**:Rybrevant应储存在2°C至8°C的冰箱中,避免光照且不要冷冻。
11. **哺乳期使用**:不建议在Rybrevant治疗期间和末次给药后3个月内进行母乳喂养。
12. **药物供应**:Rybrevant为无菌、无防腐剂、无色至淡黄色的静脉输注溶液,每瓶含有350mg/7mL (50mg/mL)。
医疗提供者将根据患者的具体情况调整治疗方案,并在整个治疗期间监测患者的反应和任何不良事件。患者应遵循医疗提供者的所有指导,并在出现任何问题时立即联系医疗提供者。